Podemos predecir como se comportará o Helio, o gas que enche o globo cando, no seu percorrido a través da troposfera e a estratosfera, a temperatura ou a presión diminúan? Que volume ocupará o gas no interior do globo cando este estoupa?
Podemos predecir como se comportará o Helio, o gas que enche o globo cando, no seu percorrido a través da troposfera e a estratosfera, a temperatura ou a presión diminúan? Que volume ocupará o gas no interior do globo cando este estoupa?
Leis dos gases
Aprende
Experiencia 1
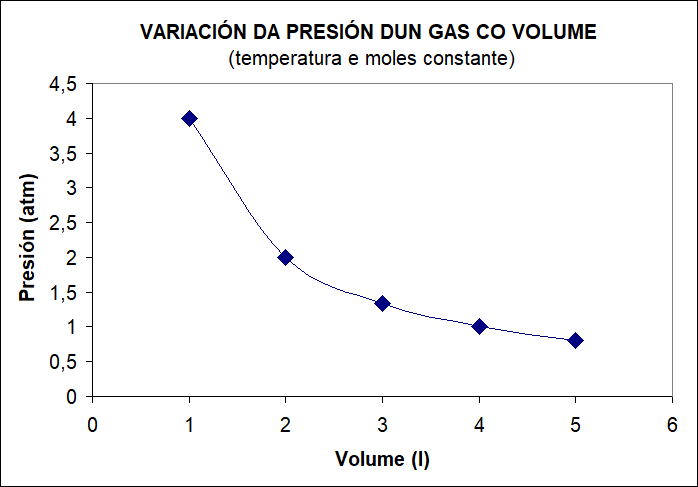
En primeiro lugar comprobamos a dependencia da presión do gas co volume que ocupa. Enchemos un recipiente cunha cantidade fixa de gas (número de moles), mantemos constante a temperatura e variamos o volume, medindo a presión do gas.
| Datos obtidos | Representación gráfica | Conclusións | ||||||||||||
|
Variación da P co V. Raquel Rendo. Commons Wikimedia. CC BY-SA-NC 4.0 |
Da análise dos datos e a súa representación gráfica podemos deducir que a presión e o volume son magnitudes inversamente proporcionais: ao facer o volume o doble a presión redúcese a metade; ao facer o volume o triple, a presión redúcese a terceira parte, etc... Isto exprésase en matemáticas mediante a función y=k/x ou o que é o mesmo: \[P\cdot V=k_{1}=cte\; \;\; ou\; \; \; P=k_{1}\frac{1}{V}\] |
Comprobamos pois que os valores do produto (P·V) toman o mesmo valor (neste caso sempre é 4) e enunciamos a lei de Boyle: "A temperatura constante, para unha determinada cantidade de gas, o produto presión por volume permanece constante".
Lei de Boyle (en video)
Ruben Sebastian. Ley de Boyle-Mariotte. En Youtube. Licencia Estándar de YouTube.
Experiencia 2
Nesta experiencia comprobamos a relación entre a presión do gas e a temperatura, mantendo constante o volume e a cantidade de gas.
| Datos obtidos | Representación gráfica | Conclusións | ||||||||||||||||||||||||
|
Variación da P ca T. Raquel Rendo. Commons Wikimedia. CC BY-SA-NC 4.0 |
Da análise dos datos e a súa representación gráfica podemos deducir que a presión e o volume son magnitudes directamente proporcionais e que, se a prolongamos, a recta que une os datos pasa pola orixe de coordenadas. Isto exprésase en matemáticas mediante a función y=k·x ou o que é o mesmo: \[P=k_{2}\cdot T\] |
O resultado desta experiencia leva a enunciar a lei de Gay-Lussac: "A volume constante, para unha determinada cantidade de gas, a presión depende directamente da temperatura".
Lei de Gay-Lussac (en video)
Ruben Sebastian. Ley de Gay-Lussac. En Youtube. Licencia Estándar de YouTube.
Experiencia 3
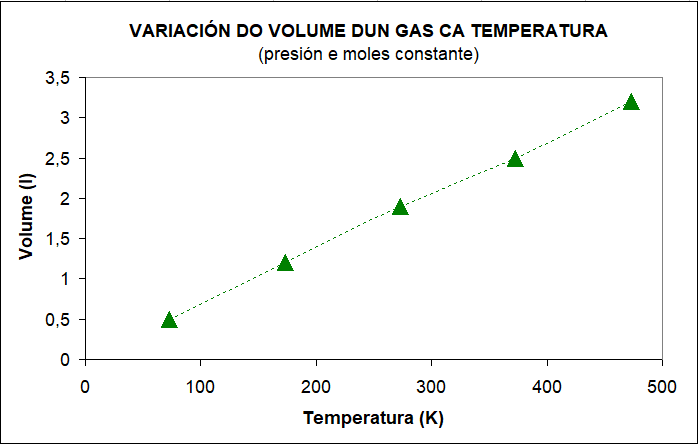
Nesta ocasión analizamos a dependencia entre o volume a temperatura: introducimos unha determinada cantidade de gas nun recipiente, mantemos constante a presión, e varíase a temperatura para ver como cambia o volume do gas.
| Datos obtidos | Representación gráfica |
Conclusións |
||||||||||||
|
Variación do V ca T. Raquel Rendo. Commons Wikimedia. CC BY-SA-NC 4.0 |
De novo a relación entre a temperatura e o volume é lineal, polo tanto: \[V=k_{3}\cdot T\] |
Lei de Charles (en video)
Ruben Sebastian. Ley de Charles. En Youtube. Licencia Estándar de YouTube.
Lei ou ecuación de estado dos gases ideais
A partir das tres experiencias anteriores e as tres leis que se enunciaron a partir delas: Boyle, Gay-Lussac e Charles, podemos enunciar a lei ou ecuación de estado dos gases ideais: para un número de partículas de calquera gas, o producto da presión polo volume dividido entre a temperatura absoluta do gas é unha constante.
|
\[\frac{P\cdot V}{T}=cte\] |
|
| Ruben Sebastian. Ecuación o Ley general de los gases ideales. En Youtube. Licencia Estándar de YouTube. |
Licenciado baixo a Licenza Creative Commons Recoñecemento Compartir igual 4.0